Die erste neue Behandlung für die Alzheimer-Krankheit seit fast 20 Jahren wurde von den Behörden in den USA zugelassen und ebnet damit den Weg für ihren Einsatz in Großbritannien.
Aducanumab zielt auf die zugrundeliegende Ursache der Alzheimer-Krankheit, der häufigsten Form der Demenz, und nicht auf deren Symptome.
Wohltätigkeitsorganisationen haben die Nachricht über eine neue Therapie für die Krankheit begrüßt.
Aber die Wissenschaftler sind wegen der Unsicherheit über die Studienergebnisse geteilter Meinung über die möglichen Auswirkungen.
Mindestens 100.000 Menschen in Großbritannien mit einer milden Form der Krankheit könnten für das Medikament geeignet sein, wenn es von der britischen Behörde zugelassen würde.
Die US-amerikanische Food and Drug Administration (FDA) sagte, es gebe „substanzielle Hinweise darauf, dass Aducanumab die Amyloid-Beta-Plaques im Gehirn reduziert“ und dass dies „mit einiger Wahrscheinlichkeit wichtige Vorteile für die Patienten erwarten lässt“.
Umstrittener Prozess
Im März 2019 wurden internationale Studien in der Spätphase mit Aducanumab, an denen etwa 3.000 Patienten teilnahmen, gestoppt, als die Analyse zeigte, dass das Medikament, das als monatliche Infusion verabreicht wird, die Verschlechterung von Gedächtnis- und Denkproblemen nicht besser verlangsamt als ein Scheinmedikament.
Doch später im Jahr analysierte der US-Hersteller Biogen weitere Daten und kam zu dem Schluss, dass das Medikament tatsächlich wirkte, solange es in höheren Dosen verabreicht wurde. Das Unternehmen sagte auch, dass es den kognitiven Verfall deutlich verlangsamt.
Aducanumab richtet sich gegen Amyloid, ein Protein, das im Gehirn von Menschen mit Alzheimer abnorme Klumpen bildet, die Zellen schädigen und Demenz auslösen können:
- Gedächtnis- und Denkprobleme
- Kommunikationsfragen
- Verwirrung
‚Auf dem Weg in die richtige Richtung
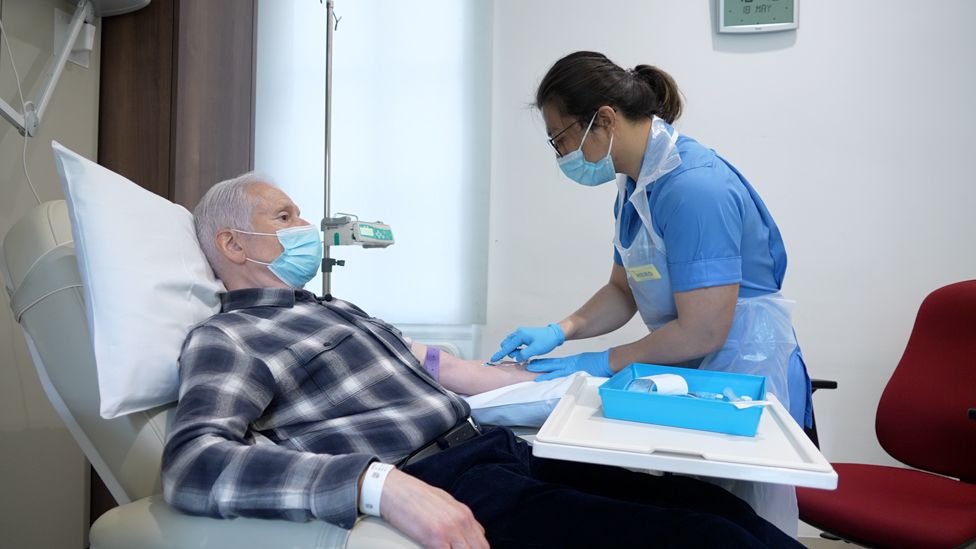
Aldo Ceresa, der an der Studie teilnahm, bemerkte erstmals vor 10 Jahren Probleme bei der Unterscheidung zwischen links und rechts.
Nach der Diagnose musste der 68-Jährige, der ursprünglich aus Glasgow stammt und jetzt in Oxfordshire in der Nähe seiner Familie lebt, seinen Job als Chirurg aufgeben.
Herr Ceresa nahm zwei Jahre lang Aducanumab ein, bevor die Studie abgebrochen wurde – und musste dann fast genauso lange auf den Beginn einer weiteren Studie am National Hospital for Neurology and Neurosurgery in London warten.
„Ich bin sehr froh, dass ich mich freiwillig melde“, sagt er.
„Ich genieße diese Reise, die ich durchmache, wirklich sehr – und natürlich die Vorteile, die ich daraus ziehe, wofür ich sehr, sehr dankbar bin.“
Er ist überzeugt, dass das Medikament ihm geholfen hat.
„Ich habe das Gefühl, dass ich nicht ganz so verwirrt bin. Obwohl es immer noch da ist, ist es nicht ganz so schlimm.
„Und ich werde jetzt einfach ein bisschen selbstbewusster.“
Herr Ceresa sagt, dass auch seine Familie Verbesserungen bemerkt hat.
„Wenn ich früher etwas holen wollte, wusste ich nicht mehr, wo ich die Sachen in der Küche finde.
„Das ist weniger ein Problem geworden“, sagt er.
„Ich habe noch nicht das Niveau erreicht, das ich früher hatte – aber ich bin auf dem richtigen Weg.“
Man geht davon aus, dass weltweit mehr als 30 Millionen Menschen an Alzheimer erkrankt sind, die meisten davon im Alter von über 65 Jahren.
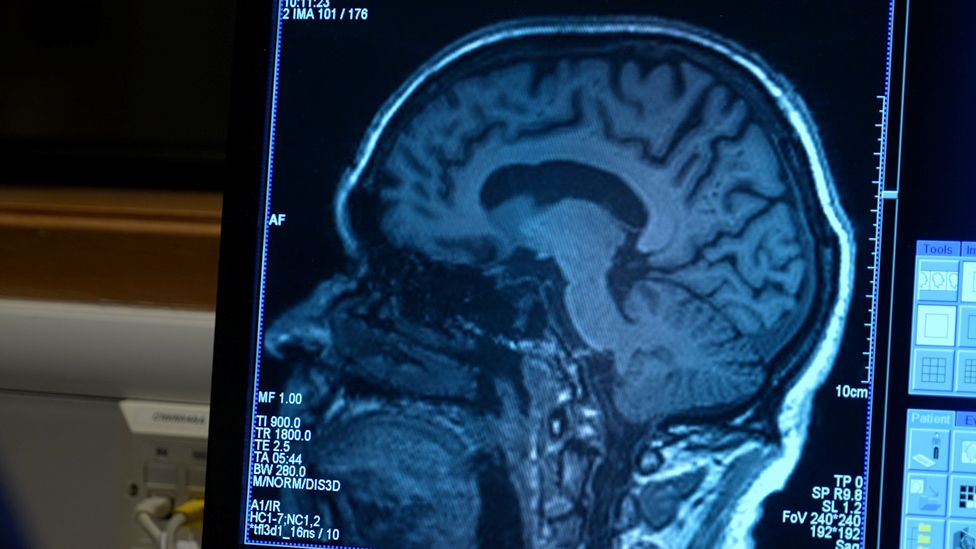
Bei den rund 500.000 Betroffenen in Großbritannien sind diejenigen, die für Aducanumab in Frage kommen, meist über 60 oder 70 Jahre alt und befinden sich in einem frühen Stadium der Erkrankung.
‚Sehr vorsichtige Feier‘
Wir müssen mit den Füßen auf dem Boden bleiben.

Dies ist kein Wundermittel und auch keine Heilung für Alzheimer, aber es ist die erste Behandlung, die den zerstörerischen Mechanismus im Gehirn angreift, der die Zerstörung der Neuronen antreibt.
Und das macht diesen Moment zu einem Meilenstein.
Doch die wissenschaftliche Meinung sowohl hier als auch in den USA ist geteilt. Während die einen die Zulassung begrüßen und sie als Meilenstein für Millionen von Alzheimer-Patienten bezeichnen, glauben andere, dass das Medikament nur einen geringen Nutzen haben wird.
Alzheimer-Organisationen sagen, dass sie auf eine baldige Entscheidung in Großbritannien drängen werden – aber das könnte noch ein Jahr dauern.
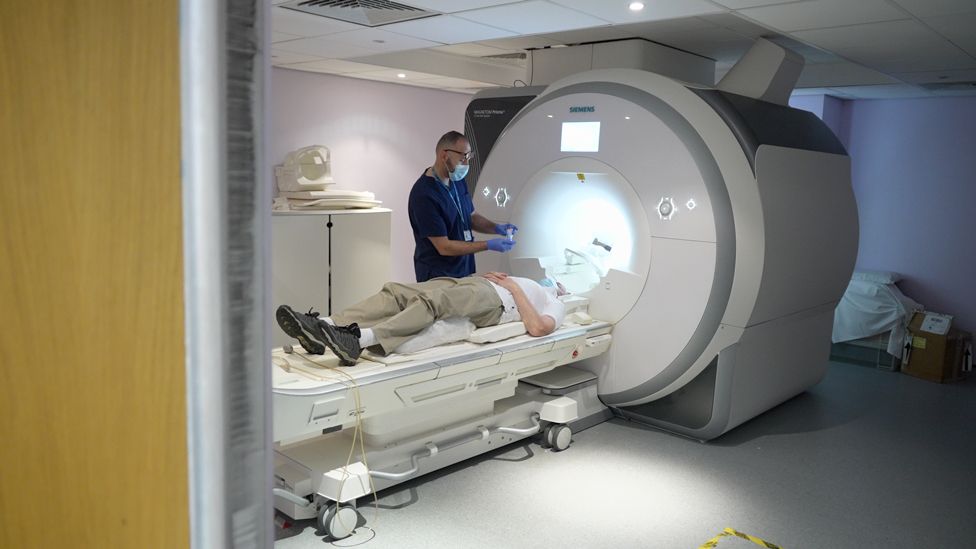
Und schließlich wissen wir nicht, wie viel Aducanumab kosten wird – es könnten Zehntausende von Pfund pro Patient und Jahr sein. Und wenn es zugelassen wird, wird der Zugang auf diejenigen beschränkt sein, die sich einer speziellen Hirnuntersuchung unterzogen haben, um ihre Diagnose zu bestätigen.
Trotz aller Vorbehalte ist dies ein Moment für sehr vorsichtiges Feiern.
Prof. Bart De Strooper, Direktor des UK Dementia Research Institute, sagte, die Entscheidung, Aducanumab zuzulassen, markiere „einen enorm wichtigen Meilenstein“ bei der Suche nach Behandlungsmöglichkeiten für die Alzheimer-Krankheit.
In den letzten zehn Jahren sind mehr als 100 potenzielle Alzheimer-Therapien gescheitert.
Aber während er hoffte, dass sich dies als Wendepunkt für Millionen von Menschen mit der Krankheit erweisen würde, sagte er, dass es „noch viele Barrieren zu überwinden“ gäbe.
Prof. John Hardy, Professor für Neurowissenschaften am University College London, sagte: „Wir müssen uns darüber im Klaren sein, dass dies bestenfalls ein Medikament mit marginalem Nutzen ist, das nur sehr sorgfältig ausgewählten Patienten helfen wird.“
Schwerer Fehler
Und Prof. Robert Howard, Professor für Alterspsychiatrie am UCL, ging noch weiter und nannte die Zulassung des Medikaments „einen schweren Fehler“, der die laufende Suche nach sinnvollen Demenzbehandlungen „für ein Jahrzehnt“ entgleisen lassen könnte.
Er sagte, die FDA habe Daten aus der Studie ignoriert, die keine Verlangsamung des Rückgangs der Kognition oder Funktion zeigten.
Die Alzheimer’s Society bezeichnete das Medikament jedoch als „vielversprechend“, fügte aber hinzu, dass es „nur der Anfang des Weges zu neuen Therapien für die Alzheimer-Krankheit“ sei.
Eine andere Wohltätigkeitsorganisation, Alzheimer’s Research UK, teilte mit, sie habe an den Gesundheitsminister Matt Hancock geschrieben und die Regierung gebeten, dem beschleunigten Zulassungsverfahren für das Medikament in Großbritannien Priorität einzuräumen.
Geschäftsführerin Hilary Evans, sagte: „Menschen mit Demenz und ihre Familien haben viel zu lange auf lebensverändernde neue Behandlungen gewartet.
„Es ist jetzt wichtig, dass die Zulassungsbehörden die Beweise bewerten, um zu entscheiden, ob sie das Medikament für die Verwendung in Großbritannien für sicher und wirksam halten.“
Obwohl viele Ärzte am Nutzen von Aducanumab zweifeln, könnte seine Zulassung in den USA der Demenzforschung, die im Vergleich zu Krebs oder Herzerkrankungen traditionell unterfinanziert ist, einen enormen Schub geben.

